빛은 파동성을 가진다.
하지만 입자성도 가진다.
이런 주장은 처음에 엄청난 저항과
무시를 받았지만, 현대 과학의 새로운
패러다임을 만들어냈다.
파동은 빛 에너지가 마치 물결처럼
일정한 굴곡을 가지고 그 굴곡에 의해
파장에 따른 색에 차이를 보이는 특성이다.
반면
입자는 '물질'이다. 그러므로 다른 물질에
충돌하여 에너지를 전달하고 움직이게 한다.
어떻게 둘은 공존할 수 있을까?
1. 빛의 입자성
빛의 알갱이는 하나하나 셀 수 있고
이를 '광자'(C)라고 한다.

입자 하나의 에너지를 'E'라고 본다면
'E=hv'라는 식이 성립한다.
v는 저번 글에서 '빛의 진동수'라고 했는데
h는 무엇을 나타내는 것일까?
바로 플랑크 상수이다.
플랑크 상수로 부터 양자역학이 시작되었다.
2. 플랑크 상수 (Plank Constant)
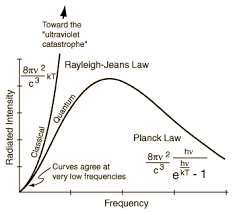
위 그래프 자료를 살펴보면
Classical과 Quantum이라고 적힌 그래프가 있다.
빛을 파동이라고만 인식하고 만들어진
고전 역학적인 식(Classical)으로는 더 이상
* 양자(Quantum) 곡선을 설명할 수 없었다.
* 양자: 어떤 양이 단위량의 정수배를 나타날 때의 단위량
따라서 '플랑크'라는 학자가 식을 완벽하게
맞추기 위해서 '에너지는 특정한 값의 정수배를
가지고 있다' 가정하고 그림 오른쪽 아래에 있는
'플랑크 상수'를 만들었다.
플랑크가 만들어 낸 상수로 양자의 곡선과
같은 곡선을 유도해냈고 이는 E=nhv라는
식으로 표현이된다.
* n 은 '정수배'라는 뜻으로 양자화를 설명한다.
하지만 고전역학의 신봉자였던 플랑크는
이런 공식을 인정하지 못하고 죽을 때까지
하나의 '가정'일뿐이다라고 말하며 생을 마감하였다.
이때 아인슈타인이 등장한다.
3. 아인슈타인의 광양자 가설

광전효과의 실험을 간단히 실험하면 이렇다.
금속판에 빛 에너지를 쏘게 되면
특정 양의 전자를 방출한다.
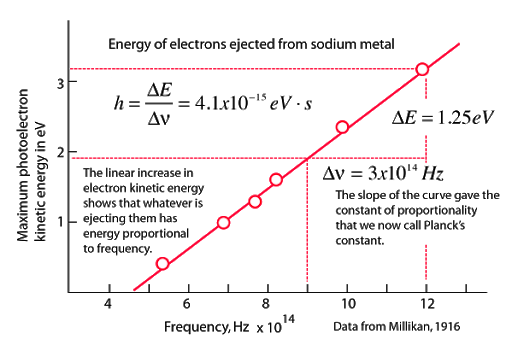
하지만 빛의 진동수가 일정 역치 값을 넘지
못하면 전자는 방출되지 않았다.
만약 빛이 파동이라면 오랜 시간 금속판을
쏘았을 경우 빛이 방출되어야 하는데
그러지 못한 것이다.
즉, 빛의 밝기보다는 빛의 진동수가 중요하고
이를 식으로 표현하면 다시 'E=nhv'가 나온다.
따라서 아인슈타인은
빛은 입자이면서 동시에 파동이라는 것을 밝혀내었고
이 실험을 통해 '광양자 가설'을 발표한다.
빛의 입자성을 통해 우리는 원자의 구조를
알아갈 수 있으며, 이런 접근은 현대 과학의 기본이 된다.
정리
이번 글에서는 빛의 입자성에 대한
역사적 흐름을 조금 다뤘습니다.
깊게 들어가면 훨씬 더 많은 학자들과
이론들이 많지만 교양 수준으로 가볍게
다루기 위해 중요한 정보만 뽑아 왔습니다.
만약 더 궁금하신 분들은
1. 흑채 복사 (Blackbody radiation)
2. 플랑크 상수(Plank Constant)
이 두 가지를 더 찾아 심화학습을 추천드립니다.
오늘도 좋은 정보 얻어가셨나요?
좋아요와 구독하기 부탁드릴게요!
'화학' 카테고리의 다른 글
| 화학. 전자, 원자핵, 양성자의 발견과 원자 모델 (탐슨 음극선 실험, 러더퍼드 알파입자 실험, 전자기파, 양자역학, 고전역학) (0) | 2020.07.22 |
|---|---|
| 화학. 고전역학과 양자역학의 차이점, 드 브로이의 물질파, 빛의 이중성, 전자의 이중성, 이중 슬릿 실험 (연속성과 불연속성) (0) | 2020.07.21 |
| 화학. 오비탈 개념, 빛의 파동성 (파장, 진동수, 전자기파, 자외선, 적외선, 양자역학) (1) | 2020.06.30 |
| 화학. 원자의 특성, 분자와 이온, 공유결합, 이온결합 (동위원소, 전기 음성도, 극성 물질, 비극성 물질, 물의 특성) (0) | 2020.06.29 |
| 화학. 원소, 원자 정의와 차이점 (원소 기호표, 주기율표, 혼합물, 화합물) (0) | 2020.06.28 |




댓글